De stralende zon
Om te begrijpen wat ozon doet, kunnen we het beste beginnen bij de straling waar de ozonlaag ons tegen beschermt. De zon straalt namelijk een breed spectrum aan verschillende golflengtes van licht uit. Onze ogen zijn maar gevoelig voor een klein deel van dit totale zonlicht. Straling met een golflengte die lánger is dan zichtbaar licht (infrarood licht) kunnen we niet zien, maar wel voelen als warmte. Straling met een kórtere golflengte dan zichtbaar licht, zogeheten ultraviolet of uv-licht, kunnen we niet altijd meteen voelen, maar is wel schadelijk voor levende wezens.
Hoeveel licht de zon uitzendt per golflengte kun je goed bepalen door aan te nemen dat de zon een zogeheten zwarte straler is. Zo’n ‘ideale straler’ zendt, bij een bepaalde temperatuur, voor iedere mogelijke golflengte de maximaal mogelijke energie per oppervlakte-eenheid uit. Dit geeft een stralingsspectrum met een karakteristieke vorm, de grijze kromme in afbeelding 1. Hoeveel straling een zwarte straler uitzendt, en bij welke golflengte het maximum van het spectrum zit, hangt af van zijn temperatuur. De effectieve temperatuur van de straling die de zon uitzend ligt rond 5505 graden Celsius (oftewel zo’n 5780 Kelvin). De aarde, vanuit de ruimte gezien, lijkt ter vergelijking meer op een zwarte straler met een effectieve temperatuur van zo’n -20 ˚C.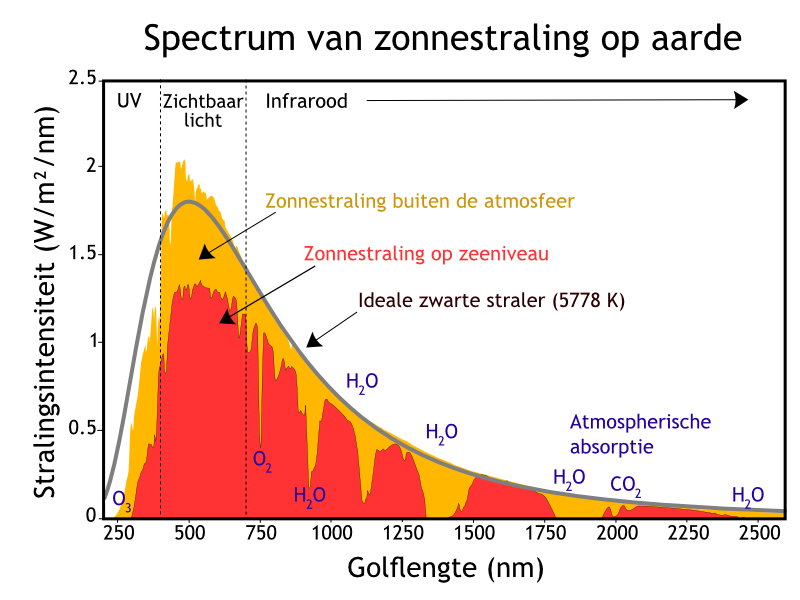
Afbeelding 1. Het stralingsspectrum van de zon.Het zonnespectrum lijkt veel op dat van een ideale zwarte straler (grijze lijn). Aan het verschil tussen de gele en oranje oppervlakken is duidelijk te zien hoeveel straling de atmosfeer absorbeert. De moleculen in de atmosfeer die hiervoor verantwoordelijk zijn, zijn aangegeven in blauw. Afbeelding: Nick84, aangepast.
In afbeelding 1 is duidelijk te zien dat de atmosfeer veel invloed heeft op de hoeveelheid van de totale zonnestraling die het aardoppervlak bereikt. Onze atmosfeer is bijzonder goed in twee dingen, namelijk warmte vasthouden, en de straling van de zon minder schadelijk maken. Dat eerste is staat bekend als het broeikaseffect. Het effect ontstaat doordat moleculen in de atmosfeer erg goed zijn in het opvangen van warmtestraling: infrarood licht, met lange golflengtes. Dit is goed te zien in het verschil tussen de gele en de rode oppervlakken aan de rechterkant van de piek in afbeelding 1. Door uitgaande warmtestraling van de aarde te absorberen en weer uit te zenden in alle richtingen, dus ook weer terug naar de aarde, werken broeikasgassen als een soort verwarmende deken om de aarde heen.
Ultra-verbrandend
Hoewel we het tegenwoordig vaak hebben over de ernstige gevolgen van klimaatverandering – veroorzaakt door onze overmatige uitstoot van broeikasgassen – redt ozon ons juist van de gevaarlijke straling aan het ándere einde van het spectrum: uv-straling. Dit licht is gevaarlijk, omdat het per eenheid méér energie overdraagt dan licht met langere golflengtes. Uv-straling bevat genoeg energie om de chemische bindingen in onze cellen open te breken, en ze daarmee flink te beschadigen. Dit kan kankerverwekkend zijn wanneer het DNA in onze huidcellen zo beschadigd raakt dat die cellen ongeremd blijven vermenigvuldigen.
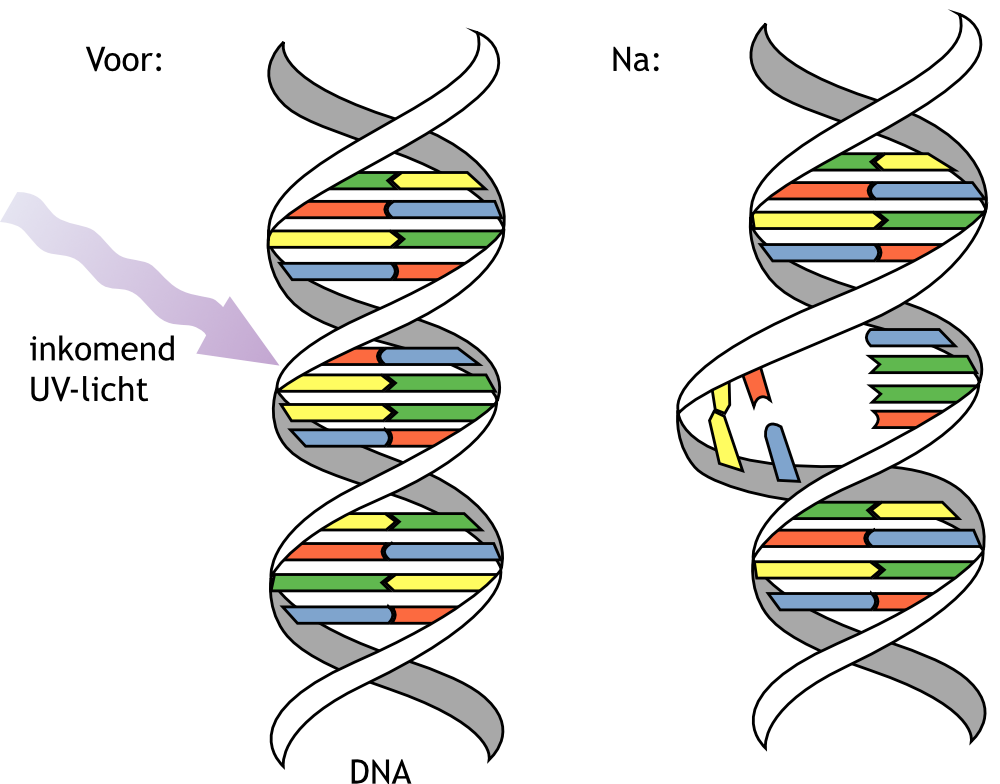
Afbeelding 2. De beschadiging van DNA door uv-straling.Uv-straling kan de chemische bindingen in moleculen zoals die van DNA breken. Afbeelding: Mouagip, aangepast.
Hoe beschadigend uv-straling is hangt sterk af van de golflengte. Hierbij geldt: hoe korter, hoe schadelijker. Toch hebben we geluk, omdat kortere golflengtes ook moeilijker door onze atmosfeer komen. En dát hebben we voornamelijk te danken aan ozon.
Een mooie cyclus
Maar wat is ozon dan precies? Als molecuul is het iets simpels: drie zuurstofatomen die aan elkaar gebonden zijn, oftewel O3. Dit in tegenstelling tot het normale zuurstofgas dat we inademen, want dat bestaat maar uit twee atomen: O2. Dat ene extra atoom maakt een groot verschil in de eigenschappen: het inademen van een concentratie van enkele ozonmoleculen per miljoen luchtmoleculen kan al dodelijk zijn! Dit komt doordat ozon heel sterk de neiging heeft om andere moleculen één of zelfs twee van zijn zuurstofatomen te geven, wat in ons lichaam zeer schadelijk kan zijn.
Hoog in de atmosfeer, voornamelijk tussen 10 en 50 kilometer boven het aardoppervlak (in de zogeheten stratosfeer), is het de giftige ozon echter onze redder. Het neemt daar alle schadelijkste uv-straling op, waarmee het zichzelf als het ware continu opoffert en herboren wordt, zoals weergeven in afbeelding 3.
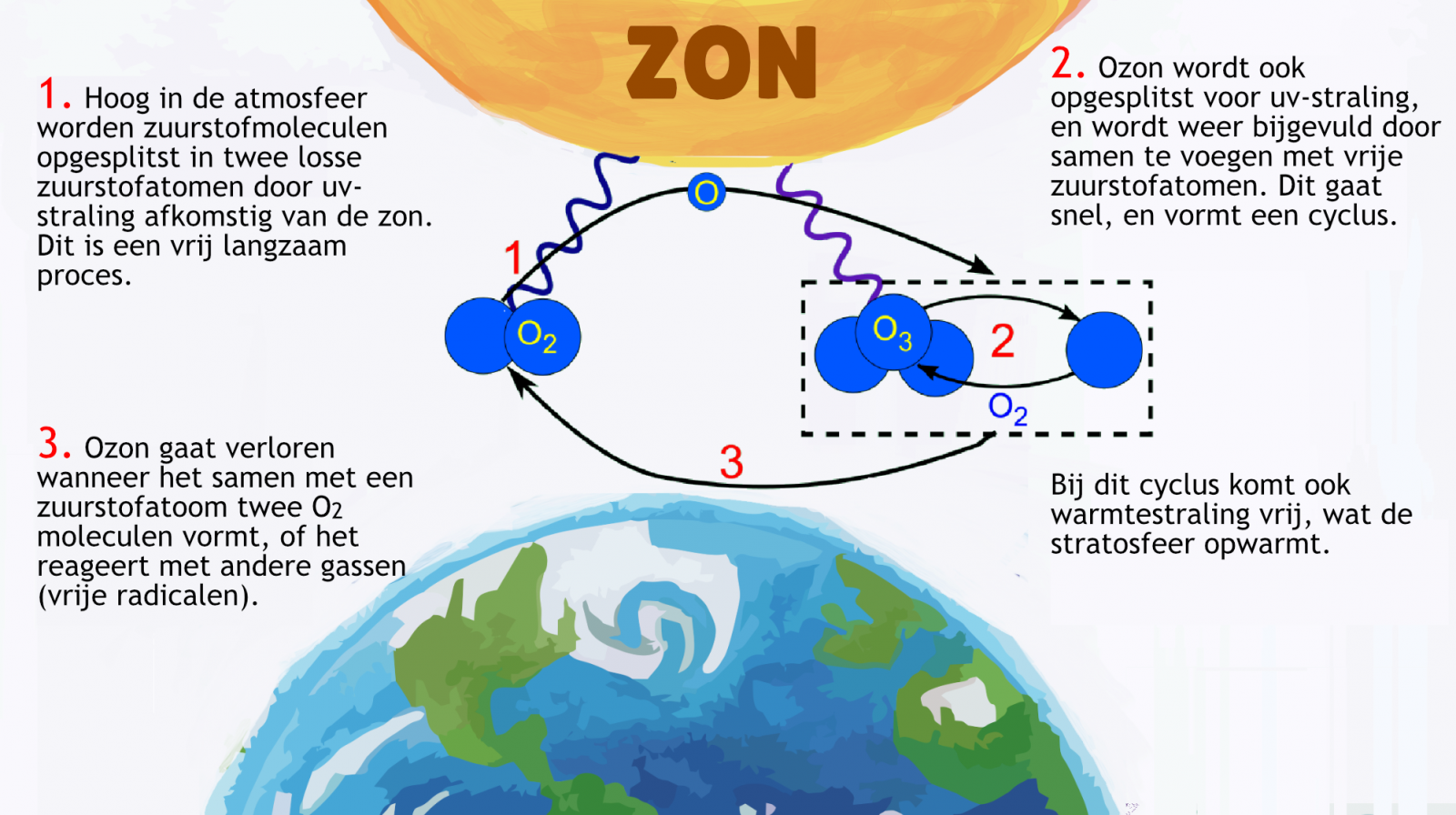
Afbeelding 3. De ozoncyclusDe ozoncyclus (stap 2) kan in het kort worden beschreven met de chemische vergelijking O3 + uv-straling ↔ O2 + O. Afbeelding: Yoshua Rameli Adan Perez, aangepast.
De reden dat we ozon nodig hebben om de sterkere uv-straling te absorberen, is zijn reactiviteit. Doordat ozon minder stabiel is dan zijn broertje O2, wordt het ook een stuk makkelijker opgebroken door de inkomende uv-straling. Door steeds weer samen te voegen met vrije zuurstofatomen, herhaalt dit proces zich, en wordt er meer uv-straling geabsorbeerd.
Een kwestie van balans
De kringloop van ozon is millennialang zonder problemen doorgegaan, maar in de tweede helft van de vorige eeuw werd het duidelijk dat wij hier de balans van in gevaar hebben gebracht. Met ‘wij’ bedoel ik slimme mensen die met moderne chemische technieken handige nieuwe stoffen ontwierpen. Een belangrijke klasse van zulke stoffen heet chloorfluorkoolwaterstoffen, cfk’s in het kort. Deze moleculen bevatten één of twee koolstofatomen, verbonden aan meerdere chloor-, fluor- en soms broomatomen. Omdat ze zo buitengewoon stabiel en niet ontvlambaar waren, werden cfk’s veelvoudig gebruikt in toepassingen waar gassen bijvoorbeeld onder druk stonden. Denk hierbij aan koelmiddelen, drijfgassen in spuitbussen en oplosmiddelen.
Het probleem was dat de eenmaal ontsnapte cfk-gassen zó stabiel waren dat ze ook hoog in de atmosfeer eindigden. Waar wetenschappers en uitvinders toentertijd nog niet aan gedacht hadden, was wat er zou gebeuren wanneer zulke moleculen sterke uv-straling tegenkomen. Ondanks hun stabiliteit worden sommige cfk’s daardoor namelijk alsnog opgesplitst, waarbij er een chlooratoom vrij kan komen dat ozonmoleculen maar al te graag opbreekt om er een zuurstofatoom van te stelen. Komt zo’n ClO-molecuul nog een vrij zuurstofatoom tegen, dan vormen de twee zuurstofatomen samen een stabiel zuurstofmolecuul (O2), en gaat het chlooratoom weer op pad om meer ozonmoleculen op te splitsen. Één vrij chlooratoom kan zo wel 100.000 ozonmoleculen vernietigen!

Afbeelding 4. Hoe één cfk-molecuul heel veel ozon kan vernietigen.Afbeelding: University of Alaska, https://theozonehole.com/ozonedestruction.htm
Een gat in de lucht spuiten
In 1974 werd de eerste link gelegd tussen cfk’s en een vermindering in de hoeveelheid ozon in de poolregio’s. Met meer metingen werd duidelijk dat er rond Antarctica gedurende grote delen van het jaar een groeiend ‘gat’ in de ozonlaag ontstond: een grote regio waar minder ozon werd waargenomen dan ooit tevoren (afbeelding 5). Als de vernietiging van de ozonlaag zo was doorgegaan, zou het desastreus zijn geweest voor al het leven op aarde.
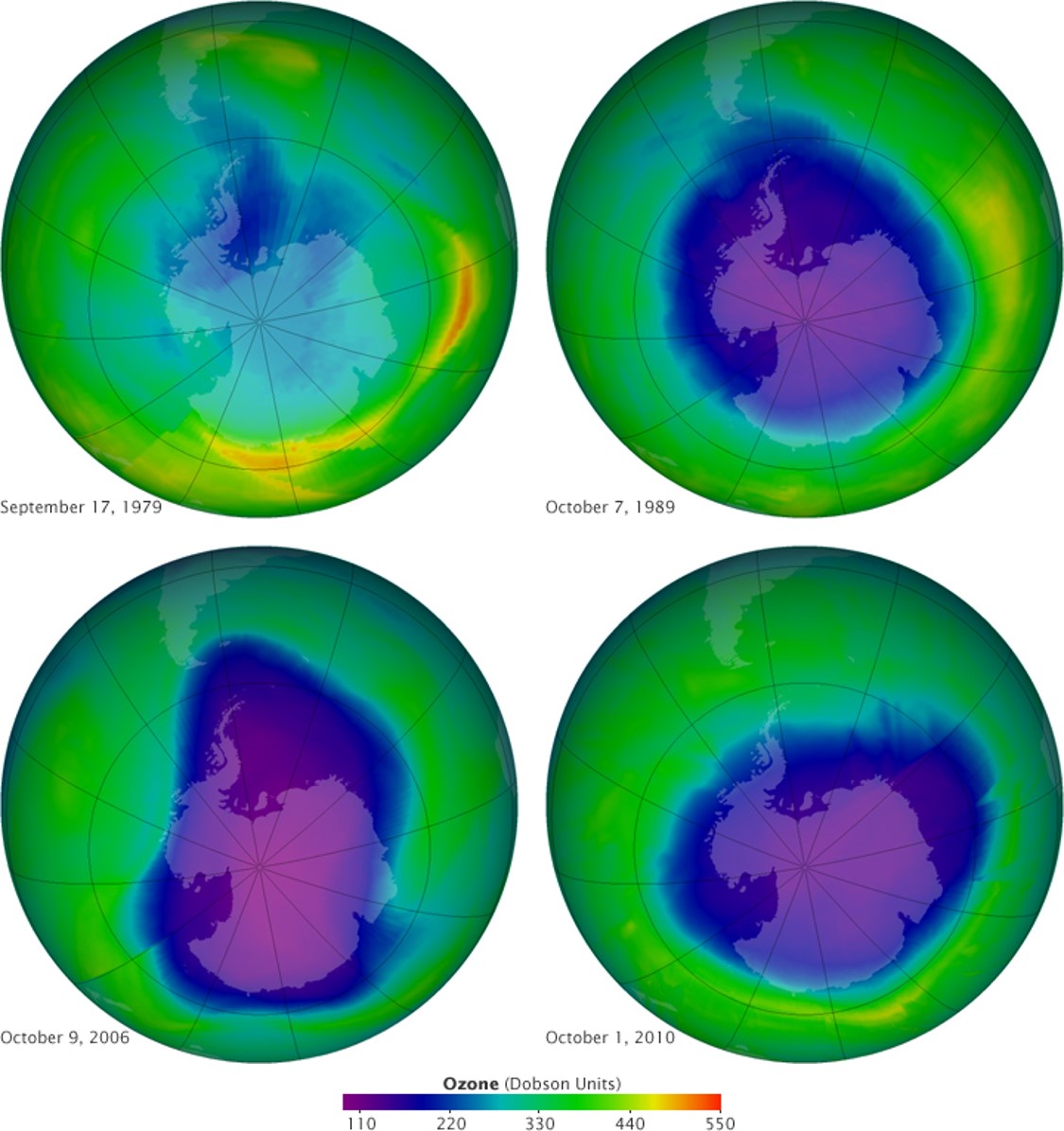
Afbeelding 5. Het gemeten gat in de ozonlaagAfbeelding: NASA Earth Observatory.
Gelukkig kwamen overheden van de hele wereld hiervoor bijeen, en spraken in de jaren 80 het zogeheten Montreal Protocol af om cfk’s te verbannen. Omdat cfk’s zo lang-levend zijn, en omdat ozon maar langzaam bijgemaakt wordt, zal het nog wel lang duren voordat de ozonlaag weer helemaal hersteld is.
Toch is er licht aan het eind van de tunnel: de laatste paar jaar lijkt het erop dat het ozongat wel weer aan het krimpen is. En ander goed nieuws: het Montreal Protocol is in 2016 ook aangepast om ook de cfk-vervangende hydrofluorkoolstoffen (hfk’s) te verbieden. Ditmaal niet voor de bescherming van de ozonlaag, maar omdat deze stoffen sterke broeikasgassen zijn. Hopelijk lukt het ons om de broeikasgasbalans ook op tijd te herstellen om catastrofale klimaatverandering te stoppen. Dan pas hebben we het hele stralingsspectrum weer onder controle.
Artikelfoto: Phil Kates.