Over de rol van Hendrik Lorentz als grondlegger van Einsteins relativiteitstheorie verscheen onlangs een artikel op deze website. Hij kreeg echter de Nobelprijs voor de natuurkunde uit 1902 die de verklaring gaf van een experiment van zijn student Pieter Zeeman. Hun ontdekkingen waren een belangrijke stap in de ontwikkeling van de quantummechanica. Zo is Lorentz wegbereider geweest voor niet één maar twéé grote revoluties in de natuurkunde van de 20e eeuw.

Afbeelding 1: Hendrik Lorentz.Foto bij de Nobelprijs 1902.
Om de fascinerende ontdekking van Zeeman en de verklaring van Lorentz te begrijpen, helpt het om alvast vooruit te denken aan de komende koude winternachten, wanneer het brandhout weer van stal gehaald kan worden. Wie wel eens een pook te lang in de open haard heeft laten liggen, weet dat materialen licht kunnen uitzenden als je ze warm genoeg maakt. De uitdrukkingen ‘roodgloeiend’ en het daarop volgende ‘witheet’ maken duidelijk dat de kleur van het licht wat uitgezonden wordt, afhangt van de temperatuur van het materiaal en daarmee van de energie van de atomen in het materiaal.
In de negentiende eeuw was het echter ook al een tijd bekend dat chemische elementen zoals waterstof en natrium in zekere zin een eigen kleur hebben. Daarmee bedoelen we niet de kleur van zo’n element in poedervorm, die is vaak gewoon wit, maar een iets minder opvallende eigenschap.

Afbeelding 2: Pieter Zeeman.Foto bij de Nobelprijs 1902.
Tegenwoordig weten we dat atomen bestaan uit elektronen die om een geladen kern van protonen en neutronen draaien. De hoeveelheid protonen bepaalt met welk element we te maken hebben. De elektronen kunnen alleen in bepaalde ‘schillen’ om de atoomkern bewegen, en de afstand tussen deze schillen hangt af van het aantal protonen in de kern en verschilt dus per element. Er zit dus een bepaalde afstand tussen de mogelijke energieniveaus van een elektron om de atoomkern.
Stel je nu voor dat een lichtdeeltje tegen een stilstaand atoom botst. Omdat het atoom zwaar is, zal het meestal niet merkbaar verplaatsen. De elektronen die om de kern draaien zijn echter veel lichter en zullen door de botsing gaan trillen. Hierdoor absorberen ze het lichtdeeltje Doordat ze echter uitsluitend over hun vaste schillen mogen bewegen, zal een elektron alleen lichtdeeltjes kunnen absorberen waarvan de energie ze precies naar een andere schil kan brengen. De lichtdeeltjes van deze energie corresponderen met een bepaalde kleur, en zo komen we tot de conclusie dat atomen bepaalde kleuren kunnen hebben. Als je licht door een gas schijnt, zullen precies de lichtdeeltjes van deze kleur door het gas geabsorbeerd worden. De karakteristieke lijnen die dit in het spectrum van het doorgelaten licht trekt, heten de spectraallijnen van het bijbehorende atoom.
![]()
Afbeelding 3: Absorbtielijnen.Bron: Wikimedia.
Buiten in het absorberen van licht komen deze spectraallijnen ook naar voren als je een gas van zulke atomen opwarmt. Het gas zal alleen licht van de spectraallijnen van zijn atomen uitzenden. Zowel het licht wat een gas uitzendt als het licht dat het absorbeert is dus in zekere zin een vingerafdruk van de bijbehorende atomen. Door deze vingerafdrukken te bekijken, wat ook wel spectroscopie wordt genoemd, worden elke dag gassen geïdentificeerd – van de nevels van sterrenstelsels tot verdachte stoffen in politieonderzoek.
Hoewel de samenstelling van atomen in de tijd van Lorentz en Zeeman nog niet op deze manier begrepen was, kende men wel al de spectraallijnen van verschillende stoffen. Pieter Zeeman kwam in 1896 op het idee om het effect van een magneetveld op deze spectraallijnen te onderzoeken. Tot zijn grote verbazing ontdekte hij dat de spectraallijnen verbreden onder invloed van een sterk magneetveld! In plaats van één strakke kleur observeerde hij een waziger spectrum.
De resultaten van Zeeman werden door zijn baas, Kamerling Onnes, op zaterdag 31 oktober 1897 gepresenteerd bij de Koninklijke Nederlandse Academie der Wetenschappen. Uit het archief van Zeeman (zie bronvermelding) weten we dat Hendrik Lorentz al de volgende maandag een theoretische verklaring van de verbreding van de spectraallijnen wist te presenteren. Deze verklaring leunt op de tevens door hem ontdekte Lorentzkracht op een geladen deeltje in een magneetveld.

Afbeelding 4: Muurschildering van de Lorentzkracht in Leiden.Bron: Wikimedia (Vysotsky)
Lorentz kon het effect van Zeeman verklaren aan de hand van het atoommodel. Als atomen bestaan uit elektrisch geladen deeltjes (elektronen) die om een kern bewegen, dan moeten de baan van deze deeltjes onder invloed van een magneetveld veranderen. Immers, geladen deeltjes die door een magneetveld bewegen, voelen de Lorentzkracht en hun baan wordt daardoor enigszins uitgerekt of ingedeukt, afhankelijk van de richting van het magneetveld ten opzichte van de baan van het elektron. Hierdoor verandert ook het energieverschil tussen nabijgelegen banen en daarmee de frequentie van het uitgezonden licht.
Aan de hand van deze verklaring zou je echter geen verbreding van de spectraallijnen verwachten, maar een splitsing in bijvoorbeeld twee scherpe lijnen. Naar aanleiding van Lorentz’ voorspelling deed Zeeman nieuwe experimenten waarin hij deze voorspelling bevestigde. Door deze prachtige samenloop van theorie en experiment werd een stap verder gezet in de beschrijving van atomen zoals we die vandaag de dag kennen.
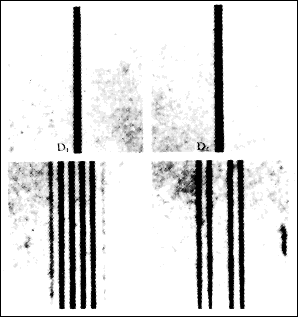
Afbeelding 5: Splitsing van spectraallijnen.Deze figuur komt uit de oorspronkelijke Nature-publicatie van Pieter Zeeman!
Meer lezen over de geschiedenis van het Zeeman-effect? Zie deze en deze artikelen van Willemien Troelstra en van Anne Kox, die in de jaren ’80 het archief van Zeeman terugvond.