
Afbeelding 1. DNA.DNA zoals we dat vandaag de dag kennen. Hoe dicht kwam Schrödingers beschrijving in de buurt? Afbeelding: MaxPixel.
In het eerste deel van dit tweeluik zagen we dat Erwin Schrödinger met behulp van biologische kennis concludeerde dat de bouwstenen van genetisch materiaal uit minder dan een miljoen atomen bestaan, maar dat dat genetische materiaal ook nagenoeg onveranderlijk is en dus zogenaamd “geordend gedrag” vertoont. Wat we ook zagen, was dat deze combinatie van feiten niet met klassieke natuurkunde verklaard kon worden. Alleen systemen die uit nóg veel grotere aantallen atomen bestaan, vertonen immers geordend gedrag en kunnen goed met klassieke statistische wetten worden beschreven. In dit artikel gaan we in op de oplossing die Schrödinger aandroeg en hoe hij daarmee aan de hand van natuurkundige redenatie al sommige dingen over de structuur van genetisch materiaal wist te voorspellen.
Een molecuul
Klassieke krachten kunnen de twee eigenschappen die Schrödinger over genetisch materiaal afleidde – onveranderlijkheid en bestaan uit een relatief klein aantal atomen – niet verklaren. Quantummechanica, zo beredeneerde hij, kan dat wel. De reden dat quantummechanica dat kan, berust op datgene wat aan de basis ervan ligt: quantisatie, oftewel: het feit dat grootheden in de quantummechanica vaak discreet zijn. In klassieke mechanica is de verandering van energie juist continu. Dat wil zeggen dat de energie van het systeem alle mogelijke waarden kan aannemen. Neem bijvoorbeeld een slinger: als je deze in beweging zet, zal de maximale snelheid langzaam afnemen door de weerstand van de lucht. De energie zal vanaf zijn beginwaarde alle tussenliggende waarden aannemen tot de slinger tot stilstand komt en de energie nul is. Op kleine schaal, waar de regels van de quantummechanica zichtbaar worden, verandert de energie echter niet continu maar die alleen een reeks van bepaalde waarden aannemen. We zeggen dat de energie discreet is.
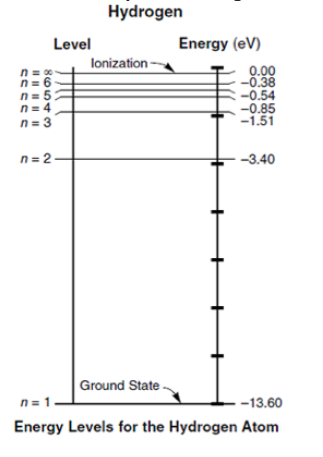
Afbeelding 2. De energieniveaus van een waterstofatoom.Een waterstofatoom kan alleen bepaalde discrete energiewaarden aannemen.
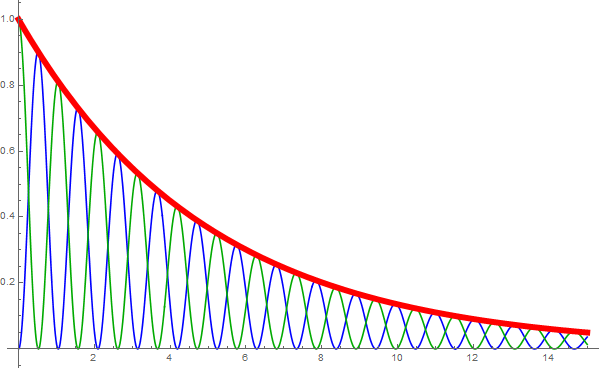
Afbeelding 3. De energie van een gedempte slinger.De kinetische (groen), potentiële (blauw) en totale energie (rood) van een slinger die in de loop van de tijd door luchtweerstand energie verliest. De totale energie neemt volgens de klassieke fysica continu af, en neemt dus alle tussenliggende waarden aan.
Bovendien hoort ieder energieniveau in een quantumsysyeem bij een bepaalde toestand van dat systeem. Daarom betekent het feit dat energie discreet is ook dat een quantummechanisch systeem alleen een reeks heel bepaalde configuraties aan kan nemen, namelijk die configuraties – of toestanden – die bij de beschikbare energiewaarden horen. Quantummechanische toestanden gaan dus niet geleidelijk in elkaar over, maar er is sprake van een ‘quantumsprong’ als toestanden in elkaar overgaan. Als de tweede toestand een hogere energie heeft, dan moet ten minste het verschil van de energie tussen de twee energieniveaus van buitenaf aan het systeem worden toegevoegd. Naar een lager energieniveau kan het systeem spontaan vervallen, waarbij de overtollige energie wordt uitgezonden in de vorm van straling.
Voor ons verhaal over genetisch materiaal is het bovenstaande belangrijk omdat de covalente binding die zich in moleculen tussen atomen bevindt ook op quantummechanica berust, zoals Walter Heitler en Fritz London in 1927 aantoonden. Dat betekent dat het ook voor moleculen onmogelijk is om een willekeurige configuratie aan te nemen. Ze kunnen alleen uit een vast aantal toestanden kiezen. Een molecuul zal zich onder normale omstandigheden in de laagste energietoestand daarvan, de grondtoestand, bevinden. Zolang het verschil in energie tussen het laagste en het op-een-na-laagste energieniveau niet aan het systeem wordt toegevoegd, zal het molecuul in die grondtoestand blijven. Het quantummechanische molecuul is daarom veel stabieler dan een eventuele klassieke tegenhanger waar Schrödinger aanvankelijk aan dacht. Ga maar na: als er aan een klassiek systeem dat zich in de laagste energietoestand bevindt een klein beetje energie wordt toegevoegd, dan zal het systeem zich direct niet meer in de toestand met laagst mogelijke energie bevinden. In een quantummechanisch systeem is een klein beetje energie daarentegen niet genoeg om het eerste energieniveau te bereiken – het zal dus in de grondtoestand blijven.
Schrödinger maakte op deze manier aannemelijk dat het basisbestanddeel van het genetisch materiaal dat zich op de chromosomen bevindt een enorm molecuul moet zijn. Een groot molecuul is een materiaal dat aan de ene kant uit relatief weinig atomen bestaat, en aan de andere kant door zijn quantummechanische aard betrekkelijk stabiel is, en dus is zo’n bouwsteen de perfecte kandidaat voor het genetisch materiaal.
Eigenlijk was deze conclusie geen groot nieuws. Het bestaan en de grote stabiliteit van moleculen was in de scheikunde al bekend en een groot molecuul werd door veel biologen al als meest waarschijnlijke kandidaat voor het genetisch materiaal beschouwd. Maar de kennis over moleculen uit de scheikunde was alleen empirisch; niemand wist precies waarom de deeltjes zo stabiel waren. Met behulp van quantummechanica kon werkelijk begrepen worden waar de stabiliteit van zo’n molecuul vandaan kwam. Wat Schrödinger ertoe bewoog om in zo’n lange verhandeling iets uiteen te zetten wat in zekere zin al bekend was, was dus vooral het feit dat hij de potentie van de quantummechanica in dergelijke vraagstukken wilde benadrukken, en zo wilde laten zien dat quantummechanica in de biologie gebruikt kon worden. Bovendien is dit niet alles. Het stuk What is life? wordt namelijk vooral geroemd om de bijna terloopse opmerking dat het grote molecuul een soort aperiodiek kristal moet zijn.
Aperiodiek kristal
Een kristal is een vaste stof met een structuur waarin de deeltjes bijzonder netjes gerangschikt zijn. De deeltjes in de structuur bewegen nauwelijks, en zijn door alle krachten die er aanwezig zijn met elkaar verbonden, net zoals een groot molecuul is verbonden door de covalente bindingen. Schrödinger stelt dat moleculen en kristallen daarom goed te vergelijken zijn. Hij onderscheidt vervolgens twee soorten kristallen: het periodieke kristal en het aperiodieke kristal. Een periodiek kristal is een structuur waarin een bepaald vast patroon van atomen steeds herhaald wordt; een aperiodiek kristal heeft een meer ingewikkelde structuur waarbij ieder atoom, of ieder groepje atomen, een individuele rol speelt. Van herhaling van hetzelfde patroon is in een aperiodiek kristal dus geen sprake.

Afbeelding 4. Een zoutkristal.Afbeelding: Benjah-bmm27.
Deze laatste beschrijving lijkt in veel opzichten op het DNA zoals we dat nu kennen: het is een soort code – regelmatig, maar niet herhalend – die “uitgelezen wordt” en de informatie draagt over bijvoorbeeld ons uiterlijk en over onze ontwikkeling. Dergelijke bewoordingen gebruikt Schrödinger in What is Life? ook al. Hij noemt het gen meermaals een code-script en had dus al door dat het genetisch materiaal uit een structuur moest bestaan waar ieder stukje zijn eigen unieke bijdrage levert. Dat inzicht leidde hem ertoe te stellen dat het grote molecuul een aperiodiek kristal moest zijn. En hoewel die conclusie nu erg voor de hand lijkt te liggen, was het destijds een groot inzicht waarvan de waarde pas erkend werd toen de werkelijke structuur van het gen ontdekt werd!